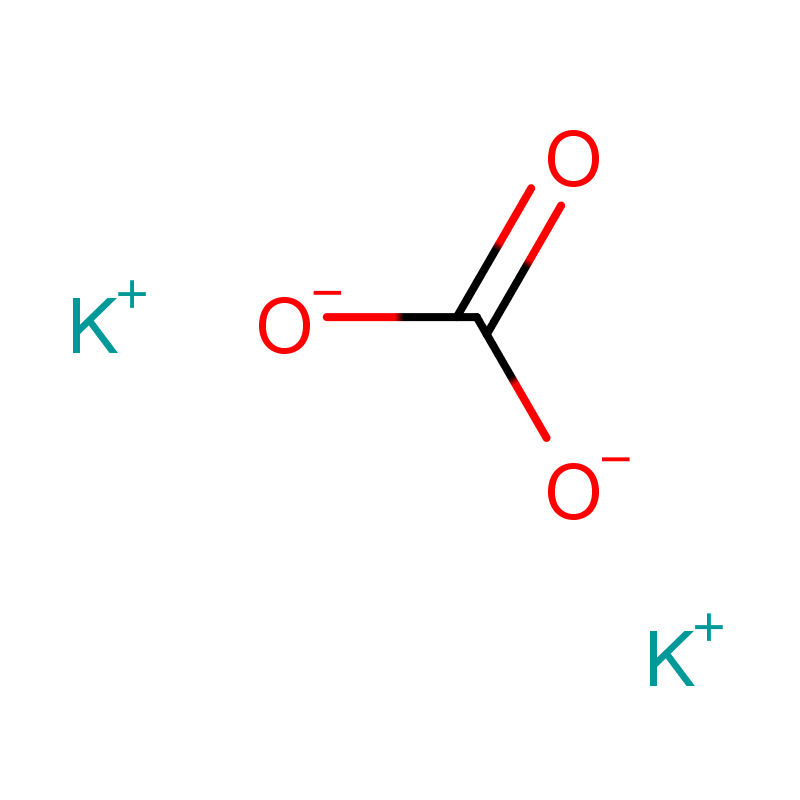
Carbonato de potasio CAS#584-08-7: El actor versátil en productos químicos
El carbonato de potasio (K₂CO₃), un compuesto inorgánico ampliamente estudiado, se ha utilizado desde la antigüedad debido a sus propiedades químicas únicas y sus diversas aplicaciones. Desde su formación natural hasta sus múltiples usos en la industria moderna, la historia del carbonato de potasio refleja el desarrollo de la química y la civilización humana.
Explorar el carbonato de potasio nos permite comprender mejor esta sustancia y apreciar el complejo papel que desempeñan las sustancias químicas en la sociedad contemporánea. Este artículo explorará las propiedades químicas, los métodos de producción y los diversos usos del carbonato de potasio, considerando también su impacto ambiental y las posibles áreas de investigación futura.
Propiedades químicas
El carbonato de potasio (K₂CO₃) es una sal blanca e higroscópica que absorbe la humedad de la atmósfera, formando una solución o hidrato cristalino. Pertenece a la familia de los carbonatos, donde dos cationes potasio se aparean con un anión carbonato.
Estable y no inflamable, el carbonato de potasio tiene un alto punto de fusión de 891 °C (1636 °F), lo que lo hace adecuado para aplicaciones de alta temperatura como la fabricación de vidrio. Es soluble en agua y su solubilidad aumenta con la temperatura, produciendo una solución fuertemente alcalina capaz de neutralizar ácidos. Esta característica se aprovecha en procesos de tamponamiento y regulación del pH.
Si bien las soluciones de carbonato de potasio son alcalinas, no constituyen una base tan fuerte como los hidróxidos. Al reaccionar con ácidos, el carbonato de potasio produce dióxido de carbono y agua, una reacción típica de los carbonatos que se utiliza en industrias como la producción de bebidas, donde se requiere la carbonatación.
A nivel molecular, el ion carbonato (CO₃²⁻) consiste en un átomo de carbono central unido a tres átomos de oxígeno en una forma trigonal plana. Las estructuras de resonancia de este ion contribuyen a su estabilidad y reactividad. Los fuertes enlaces iónicos entre los iones potasio (K⁺) y el ion carbonato mantienen el compuesto en estado sólido a temperatura ambiente.
En soluciones acuosas, el carbonato de potasio alcanza un equilibrio con el bicarbonato de potasio (KHCO₃), una reacción que depende de la temperatura. Este equilibrio es importante para comprender la capacidad amortiguadora del compuesto en diversos contextos, como en suelos y ciertos productos alimenticios.
Además, el carbonato de potasio reacciona con el dióxido de carbono para formar bicarbonato de potasio, contribuyendo al ciclo del carbono y actuando como amortiguador en los procesos ambientales. También puede interactuar con iones metálicos en solución, formando precipitados insolubles, lo cual desempeña un papel fundamental en los procesos de ablandamiento y purificación del agua.